Alzheimer araştırmacıları, onlarca yıldır tek bir hedefe odaklandı: beyindeki o yapışkan amiloid plakları ortadan kaldırmak. Bu yaklaşıma milyarlarca dolarlık yatırım yapıldı, yüzlerce klinik deney başarısızlıkla sonuçlandı. Ta ki 2026 başında Barselona Üniversitesi’nden bir ekip, tüm dengeleri değiştirebilecek bir keşif yapana kadar. Adı FLAV-27 olan bu deneysel bileşik, plakları temizlemeye çalışmak yerine beynin kendi genetik programlama mekanizmasını sıfırlıyor.
Mevcut Tedavilerin Açmazı
Alzheimer, dünya genelinde 55 milyondan fazla insanı etkileyen ve hâlâ kesin bir tedavisi bulunmayan bir hastalık. 2023 ve 2024 yıllarında FDA tarafından onaylanan lecanemab ve donanemab gibi monoklonal antikor ilaçlar, hastalığın altında yatan temel nedenlerden birini; beyin dokusunda biriken amiloid beta plakları hedef alıyor. Donanemab’ın klinik deneylerde günlük yaşam aktiviteleri (ADL) ölçeğindeki gerilemeyi %40 oranında, genel bilişsel gerilemeyi ise %35 oranında yavaşlattığı bildirildi.
Peki, elde edilen bu başarı neden asıl çözüm olarak görülmüyor? Çünkü mevcut ilaçlar, bilişsel gerilemeyi yalnızca %27 ile %35 oranında yavaşlatıyor; üstelik ciddi yan etkileri var ve hastalığın yalnızca bir bileşeni olan amiloid birikimini hedef alıyorlar. Asıl çelişki tam burada başlıyor: amiloid plaklar, semptomlar ortaya çıkmadan 20 yıl önce beynin görüntülemelerinde görülebiliyor. Plakları olan ama bilişsel kaybı hiç yaşamayan insanlar da mevcut; bu da plakların tek başına hastalığı açıklamadığına işaret ediyor. Yani mevcut ilaçlar, asıl sorunun yalnızca bir parçasıyla savaşıyor.
FLAV-27 Nedir ve Nasıl Çalışır?
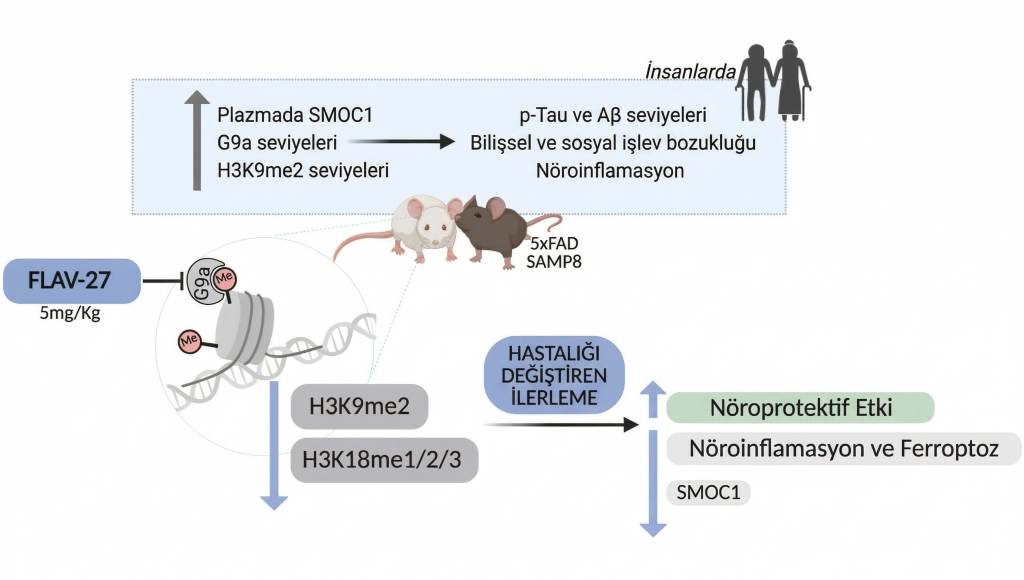
Barselona Üniversitesi’nden Prof. Christian Griñán ve Prof. Mercè Pallàs liderliğindeki ekip, tamamen farklı bir kapıyı araladı: epigenetik. Epigenetik, DNA’nın dizisini değiştirmeksizin hangi genlerin açık ya da kapalı olduğunu belirleyen kimyasal işaretlerin sistemi. Alzheimer’da bu sistem bozuluyor: hafıza güçlendirme, sinaptik plastisite ve nöronal gelişim için kritik genlerin yanlış biçimde susturulduğu görülüyor.
FLAV-27’nin hedefi G9a enzimi. Bu enzim, epigenetik yazıcılar olarak bilinen protein ailesinden biri; görevi ise beyindeki belirli genlerin üzerine kimyasal bir işaret koyarak onları susturmak. Alzheimer’da G9a aşırı aktif hale gelip hastalığın ilerlemesine katkıda bulunan genleri susturuyor. FLAV-27 ise G9a’nın DNA üzerinde işlem yapabilmesi için ihtiyaç duyduğu S-adenosilmetiyonin (SAM) adlı doğal molekülün enzime erişimini engelliyor. Böylece epigenetik düzensizlik yavaşlıyor ve nöronlar normal işlevlerine kavuşuyor.
“FLAV-27, hastalığın semptomları üzerine ya da tek bir patolojik biyobelirteç üzerine değil, doğrudan temelindeki moleküler mekanizmalar üzerine etki ediyor.“
– Aina Bellver, UBneuro araştırmacısı, makalenin yazarlarından
Hayvan Deneylerinde Ne Gördüler?
Araştırmanın sonuçlarındaki bulgular yalnızca moleküler düzeyde değil, davranışsal düzeyde de somut. FLAV-27 uygulamasının ardından deney modellerinde kısa ve uzun süreli hafızada iyileşme, uzamsal hafızanın geri kazanılması ve sosyal davranışın normale dönmesi gözlemlendi. İlaç aynı zamanda beta-amiloid ve fosforillenmiş tau proteinleri gibi Alzheimer’ın iki klasik patolojik belirtecini de azalttı. Testler yalnızca fare modeliyle sınırlı kalmadı; C. elegans isimli küçük bir solucan modelinde de hareket kapasitesi, yaşam beklentisi ve mitokondriyal solunum geliştiği görüldü.
Araştırmacılara göre bu bulgular önemli bir teorik kırılmayı da destekliyor: Epigenetik düzensizlik, Alzheimer’ın bir yan etkisi değil; beta-amiloid, tau, nöroinflamasyon ve sinaptik işlev bozukluğunu ortak bir epigenetik eksen üzerinden birbirine bağlayan aktif ve kontrol edilebilir bir mekanizma.
Kan Testi ile Tedaviyi Takip Etmek
FLAV-27’yi diğer ilaç adaylarından ayıran önemli bir başka boyut daha var: biyobelirteçler. Ekip, H3K9me2 epigenetik belirteci, SMOC1 proteini ve p-tau181 molekülünün hasta beyninde olduğu kadar kan plazmasında da yüksek düzeyde bulunduğunu keşfetti. Üstelik bu kan değerleri, FLAV-27 uygulandığında bilişsel iyileşmeyle paralel olarak normale döndü. Bu bulgu, gelecekteki klinik deneyler için son derece değerli: Basit bir kan testiyle hem uygun hastaları seçmek hem de tedavinin işe yarayıp yaramadığını izlemek mümkün olabilecek.
İnsan Deneylerine Ne Zaman Geçilecek?
Şimdilik FLAV-27 ileri preklinik aşamasında. İnsan klinik denemelerine başlamadan önce en az iki hayvan türünde düzenleyici toksikoloji çalışmaları tamamlanmalı, farmasötik formu belirlenmeli ve ilgili otoritelere klinik deneme başvurusu yapılmalı. Bu süreç yıllar alacak. Geliştirme sürecini, 2025 yılında kurulan ve FLAV-27 üzerinde özel lisansa sahip Flavii Therapeutics yan kuruluşu yürütecek.
Alzheimer’da Başka Hangi Çığırlar Açılıyor?
FLAV-27 tek başına değil. Bilim dünyası son yıllarda bu cephede birden fazla yeni cephe açtı.
Stanford Üniversitesi’nden LM11A-31: Prof. Frank Longo’nun geliştirdiği bu oral ilaç adayı, sinaptik budamayı kontrol eden p75NTR adlı reseptörü hedef alıyor. Alzheimer’da bu reseptör aşırı aktif hale gelip nöronlar arasındaki bağlantıları yok ediyor. LM11A-31, hem tau birikimini azaltıyor hem sinaptik koruma sağlıyor hem de beyindeki bağışıklık hücrelerindeki iltihabı düşürüyor. Faz 2a klinik denemelerinde insanlarda güvenli olduğu onaylandı; Faz 3 için finansman arayışı sürüyor.
Washington Üniversitesi’nden CAR-Astrosit Terapisi: Kanser immünoterapisinden ilham alınan bu yaklaşımda, beynin destek hücreleri olan astrositlere “CAR hedefleme cihazı” takılıyor ve bu hücreler amiloid plaklarını sindiren makinelere dönüştürülüyor. Mart 2026’da yayımlanan çalışmada, erken müdahalede fare modellerinde plakların tamamen önlendiği, ilerlemiş olgularda ise üç ayda %50 oranında azaldığı görüldü. Bu yaklaşım, mevcut antikor infüzyon tedavilerinin aksine tek seferlik bir müdahale olanağı sunuyor.
Harvard’dan Lityum Oroat: Yaklaşık 10 yıllık araştırmanın ürünü olan bu çalışmada, beyin dokusunda lityum eksikliği yapay biçimde oluşturulduğunda hastalık dramatik biçimde hızlandı; lityum oroat bileşiği ise fare modellerinde hem patolojiyi önledi hem de hafıza kaybını geri döndürdü.
Nanopartiküller ve Kan-Beyin Bariyeri: Barselona merkezli IBEC’ten araştırmacılar, Alzheimer’da hasarlanmış kan-beyin bariyerini nanopartiküller aracılığıyla onararak yalnızca 3 enjeksiyonla fare beyinlerindeki amiloidi hızla temizledi. İlk enjeksiyondan yalnızca bir saat sonra beyindeki amiloid miktarında %50-60’lık düşüş gözlemlendi.
Tablo: Yeni Nesil Alzheimer Yaklaşımları
Büyük Resim: Paradigma Değişimi
Plakları temizlemek yanlış bir hedef miydi? Muhtemelen hayır ama tek başına yeterli de değil. Bilim dünyasının yeni konsensüsü şuna işaret ediyor: Alzheimer, tek bir proteine bağlı bir hastalık değil; epigenetik düzensizlik, sinaptik hasar, nöroinflamasyon, damarsal bozukluk ve mitokondriyal işlev kaybını kapsayan çok katmanlı bir süreç. Bu nedenle gelecekteki tedavilerin bu farklı mekanizmaları aynı anda ya da birleşik biçimde hedef alması bekleniyor.
FLAV-27 bu açıdan yeni bir kapı aralıyor: plakları değil, plaklara yol açan ve tüm patolojik süreçleri birbirine bağlayan epigenetik programı hedef alarak. Mevcut kuşak ilaçların hastalığın yalnızca yüzeyinde kaldığını düşünürsek, bu belki de bilimin hastalığın kökenine gerçekten ulaşmaya başladığının işareti. Henüz insan deneylerinden uzaktayız ama yön doğru görünüyor.
Kaynaklar
- https://www.cell.com/molecular-therapy-family/molecular-therapy/fulltext/S1525-0016(25)01061-5
- https://medicalxpress.com/news/2026-03-experimental-alzheimer-drug-reverses-memory.html
- https://stanmed.stanford.edu/drug-slow-alzheimers-neurodegeneration
- https://www.science.org/doi/10.1126/science.aef8451
- https://scitechdaily.com/breakthrough-alzheimers-drug-rewires-the-brain-instead-of-just-clearing-plaques
- https://medicine.washu.edu/news/enhanced-brain-cells-clear-away-dementia-related-proteins
- https://www.counselheal.com/articles/60092/20260310/car-astrocytes-clear-amyloid-beta-plaques-one-shot-alzheimers-breakthrough.htm